Trennprinzip
Wenn Sie souverän agieren wollen, müssen Sie das nachfolgende von Grund auf verstanden und verinnerlicht haben!
Substanzen, die Sie dünnschichtchromatographisch untersuchen wollen, können fest oder flüssig sein. Insbesondere Flüssigkeiten dürfen aber nur eine geringe Flüchtigkeit haben, weil sie auf der Dünnschichtkarte liegen bleiben müssen und bis zum Nachweis nicht verdampft sein dürfen.
Chromatographische Methoden funktionieren immer nach dem Prinzip, dass eine mobile Phase, die zu diesem Zweck gasförmig oder flüssig sein muss, an einer stationären Phase vorbei läuft und die in der mobilen Phase gelösten Stoffe von der stationären Phase unterschiedlich stark zurück gehalten werden, wodurch es zu einer Auftrennung der Substanzen kommt. Bei der Dünnschichtchromatographie wird als mobile Phase ein Lösemittel verwendet, welches allein durch Kapillarkräfte in der stationären Phase hochsteigt, die zu diesem Zweck porös sein muss. Mit zunehmender Steighöhe nimmt die Geschwindigkeit ab, weil die Schwerkraft den Kapillarkräften entgegenwirkt. Weil die Substanzen auf der Dünnschichtkarte "laufen" heißt das verwendete Lösemittel, welches für diesen Umstand verantwortlich ist, logischerweise "Laufmittel".
Dünnschichtkarten sind in der Regel mit Kieselgel als stationärer Phase beschichtet. Bei Kieselgel handelt es sich um kondensierte Polykieselsäure, die an ihrer Oberfläche polare (Si-OH)-Gruppen enthält.
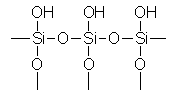
Wie bei den meisten anderen chromatographischen Verfahren auch wird also nach Polarität der zu trennenden Substanzen selektiert. Polare Stoffe adsorbieren fester auf der Kieselgeloberfläche und wandern deshalb weniger schnell als unpolare Stoffe. Man kann die Festigkeit dieser Adsorption durch die Wahl des Laufmittels beeinflussen:
- Ein polareres Laufmittel bindet seinerseits adsorptiv am Kieselgel und konkuriert also mit gelösten polaren Stoffen.
Nach Egon Stahl gilt folgendes Beziehungsdreieck:
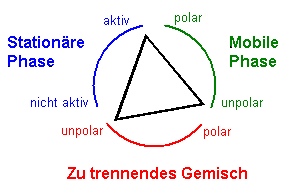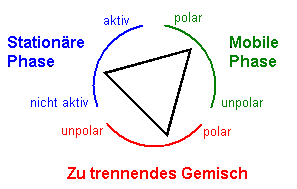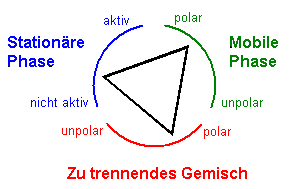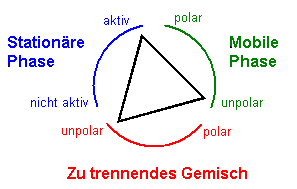
Meist - insbesondere im Praktikum werden ausschließlich Kieselgelplatten verwendet, so dass die stationäre Phase invariant ist. Die Beziehung vereinfacht sich deshalb wie folgt:
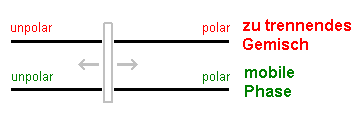
- Läuft eine Substanz zu wenig, muss die Polarität des Laufmittels erhöt werden.
- Läuft eine Substanz mit der Laufmittelfront, muss die Polarität des Laufmittels erniedrigt werden.
Unterlassen Sie alle andersartigen halbgaren Erklärungsversuche wie:
Similis similibus solvuntur - also müssten z.B. unpolare Stoffe eigentlich in unpolaren Lösemitteln besonders weit laufen und in polaren Lösemitteln hingegen besonders wenig.
Immer wieder steckt das in den Köpfen und immer wieder ist das Murks!
Tatsächlich spielt die Löslichkeit nur eine untergeordnete Rolle.
Sehr häufig wird mit Gemischen aus Hexan und Ethylacetat chromatografiert, wobei durch Erhöhung des Anteils an Ethylacetat die Polarität stufenlos erhöht werden kann. Mischungen gerade dieser beiden Lösemittel eignen sich deshalb so gut, weil deren Siedepunkte mit 69 °C bzw. 77 °C sehr ähnlich sind und bei dem bestimmungsgemäßen teilweisen Verdampfen des Laufmittels in der DC-Kammer sich die Zusammensetzung deshalb kaum ändert.

